初中化学人教版9年级上下全册知识点 - 第二单元 我们周围的空气
初中化学人教版9年级上下全册知识点 - 第二单元 我们周围的空气
第二单元 我们周围的空气
课题1 空气
一 空气是由什么组成的
1、测定空气中氧气含量实验
(1) 现象:产生白烟,集气瓶中的水上升约1/5体积.
(2) 结论:氧气约占空气体积的1/5.
(3) 实验成功的关键:
① 红磷要过量;② 容器要密封,不漏气;③ 冷却后再打开弹簧夹。
(4) 进入集气瓶中的水少于1/5的原因:
① 红磷不足,氧气未耗尽;② 瓶塞未塞紧,空气进入;③ 未冷至室温就打开弹簧夹。
(5) 进入集气瓶中的水多于1/5的原因:
①点燃红磷后伸入集气瓶的速度太慢,集气瓶中的空气受热膨胀而逸出。
②止水夹未夹紧,集气瓶中的空气受热膨胀而从导管口逸出。
(6)该实验的不足之处:
①红磷被点燃后再伸入集气瓶内,使部分空气因受热膨胀而溢出集气瓶。
②红磷在空气中点燃会污染空气。
③导管内的空气会影响实验的准确性。
(7)集气瓶中先加少量水的作用:吸收生成的五氧化二磷。
2、空气的成分按体积计算:大约是:氮气78%,氧气21%,稀有气体0.94%,CO2占0.03%,其他气体和杂质0.03%.
二 、空气是一种宝贵的资源
1 氧气用途:
(1) 供给呼吸<如登山、医疗、潜水等〉
(2) 支持燃烧<如炼钢、气焊、航空等〉
2 氮气用途:
(1) 作保护气(如汽车安全气囊、灯泡、食品袋等充氮气),利用N2化学性质不活泼.
(2) 制硝酸和化肥。(3)冷冻麻醉(4)制造低温环境。
3 稀有气体用途:
(1)电光源,利用稀有气体通电时能发出不同颜色的光。
(2)作保护气(焊接金属的保护气、灯泡内保护气),利用稀有气体化学性质很不活泼。
注意:“稀有气体”是一类气体的总称,不是一种气体。
三、保护空气
1 空气中的污染物包括烟尘和有害气体;
空气中的有害气体:CO 、 SO2 、 NO2、O3等
2 空气污染的危害:① 损害人体健康;②影响作物生长,破坏生态平衡;③全球气候变暖,臭氧破坏,酸雨。
3 防止空气污染的措施:①加强大气质量监测;②使用清洁能源;③植树造林;
④ 工厂废气处理后排放。
注意:空气污染指数包括:CO、SO2、NO2、O3、可吸入颗粒物。
四、混合物与纯净物的概念
1、混合物:宏观上由两种或多种物质混合而成的物质。微观上由两种及以上的分子构成。
2、纯净物:宏观上只由一种物质组成的。微观上由一种分子构成。
3、注意:
①、只由一种原子构成的物质不一定是纯净物。如:金刚石和石墨。
②、只含一种元素的物质可能是单质,也可能是混合物。如O2和O3的混合,只含一种元素,但是混合物。
③、纯净物都有化学式。混合物都没有化学式。
课题2 氧气
一、氧气的性质
(一) 物理性质:密度比空气大;不易溶于水;液氧和固态氧为淡蓝色
(二) 化学性质:氧气的化学性质活泼,能与多种物质发生反应,具有氧化性;氧气能支持燃烧,具有助燃性,但无可燃性。
1、S+O2 SO2
SO2
现象:空气中是淡蓝色的火焰;同时生成有刺激性气味的气体。纯氧中是蓝紫色的火焰;同时生成有刺激性气味的气体。
注意:集气瓶中装少量水的作用是吸收SO2防止污染空气。此处的水不能用沙代替。
2、3Fe+2O2  Fe3O4
Fe3O4
现象:剧烈燃烧、火星四射、放出热量、生成黑色固体。
注意:瓶中装少量水或铺一层沙的目的:防止溅落的生成物炸裂瓶底。
3、4P+5O2 2P2O5
2P2O5
现象:生成白烟,空气中燃烧产生黄色火焰,氧气中燃烧发出白光。
注意:P2O5 会污染空气。
4、C+O2  CO2
CO2
现象:空气中发出红光,放出热量,生成能够让澄清石灰水变浑浊的气体。
氧气中发出白光,放出热量,生成能够让澄清石灰水变浑浊的气体。
二、化合反应与氧化反应
1 、化合反应:(多变一)A+B==AB
氧化反应:物质与氧发生的反应叫氧化反应。
2 、关系:化合反应不一定是氧化反应,氧化反应不一定是化合反应
3、 氧化反应分类
(1)剧烈氧化:如燃烧、自燃、爆炸。
(2)缓慢氧化:如食物的腐烂、酿酒、铁生锈、呼吸作用等。
注意:
①、物质与氧气发生的反应叫氧化反应。(错)物质与氧气发生的反应是氧化反应。(对)
②、氧气中含有氧,但含有氧的物质不一定是氧气。
③、判断氧化反应的一般标准就是看反应物中是否有氧气。
课题3 制取氧气
一、氧气的实验室制法
1 药品:(1)过氧化氢、二氧化锰。(2)氯酸钾、二氧化锰。(3)高锰酸钾
H2O2 MnO2 KClO3 MnO2 KMnO4
2原理:2H2O2  2H2O+O2↑
2H2O+O2↑
2KMnO4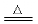 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
2KClO3 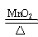 2KCl+3O2↑
2KCl+3O2↑
3 装置(以KMnO4制氧气为例)
发生装置:酒精灯、铁架台、试管。
收集装置(排水法收集):水槽、导气管、集气瓶。
4 制取步骤:连接装置→检查其密性→装入药品→固定装置→点燃酒精灯→
加热→ 收集氧气→ 将导管移出水面→熄灭酒精灯。
可以简记为:查、装、定、点、收、离、熄。
5 收集方法:排水法或向上排空气法。
6 验满方法:将带火星的木条放在集气瓶口,若木条复燃,则收集满。
7 注意:
a 铁架台的铁夹应夹在离试管口约1/3处。
b 导管伸出橡皮塞少许,不能太长。
c 用KMnO4制氧气时,试管口要放一团棉花。目的是为了防止KMnO4粉末进入导管。
d 试管口略向下倾斜。目的是为了防止冷凝水回流到热的试管底部,炸裂试管。
e 排水法收集氧气时,先将导管移出水面,再熄灭酒精灯。是为了防止水槽中的水倒吸入试管,使试管因骤冷而炸裂。
f 排水法收集时,刚开始有气泡时不能立即收集,要等气泡均匀冒出后才能开始收集气体。
g 检查气密性的方法:将导管放入水中,用手握住试管,若导管口有气泡,松开手后,导管里形成一段水柱,则证明不漏气。
二、分解反应(一变多):AB = A + B
三、催化剂:
一变:改变其它物质的化学反应速率。二不变:催化剂的质量和化学性质在反应前后不变。
注意:催化剂只改变反应速率,不改变生成物的质量多少。
◆改变反应速率可以加快,也可能是减慢反应速率。
四、工业上制氧气的方法:分离液态空气。属于物理变化。
在低温条件下,使空气转变为液态,然后蒸发,氮气沸点低,首先从液态空气蒸发出来,剩下的主要就是氧气。
五、实验室用双氧水制取氧气的优点:
1、操作简单。2、不加热,节约能源。3、反应速率快。4、易回收二氧化锰。
扫描二维码推送至手机访问。
特别声明:
本站属于公益性网站,纯粹个人原因(陪孩子学习便于查询和教授),网站部分内容收集于网络,仅供学生和老师参考、交流使用,请勿用作其他商业收费用途。
如果网站内容能给你带来提升,那便是我经营此网站的初衷。网站相关内容如有问题,请及时提出,我在此谢谢!
本站尊重原创并对原创者的文章表示肯定和感谢,如有侵权请联系删除!针对本站原创内容,本站也欢迎转载,如需转载请注明出处。