初中化学人教版9年级上下全册知识点 - 第四单元 自然界的水
初中化学人教版9年级上下全册知识点 - 第四单元 自然界的水
第四单元 自然界的水
课题1 爱护水资源
一、人类拥有的水资源
淡水紧缺的原因:1、淡水占总水量的比例小;2、生产生活用水量增加;3、水体污染。
二、爱护水资源
1、措施:① 一方面节约用水;② 另一方面防止水体污染。
2、防止水污染的措施
①加强水质监测;②工业三废要处理后排放;③农业上合理农药和化肥;④生活污水要处理后排放。
3、提高水的利用效益的方法
①生活中提倡一水多用;②农业上改漫灌为喷灌、滴灌;③工业上提倡对水的循环使用。
4 、水污染的三个来源:工业污染、农业污染、生活污染。
课题2 水的净化
一、过滤操作要领
“一贴”:滤纸紧贴漏斗内壁。若有气泡,则影响过滤的速度。
“二低”:滤纸边缘要低于漏斗口;漏斗内液面低于滤纸边缘。
“三靠”:① 烧杯紧靠玻璃棒;② 玻璃棒下端靠三层滤纸处;③ 漏斗下端靠烧杯内壁。
注意:
1、玻璃棒的作用是引流。过滤时,玻璃棒不能搅拌。
2、两次过滤后仍然混浊的原因:
①滤纸破损;②液面高于滤纸边缘;③漏斗或烧杯不干净
二、净化水的方法:①沉淀、②过滤、③吸附、④蒸馏。
1、其中吸附和蒸馏能除去可溶性杂质;四种方法都能除去难溶性固体杂质。
2、沉淀包括静置沉淀和吸附沉淀。
3、净化程度由低到高的顺序:沉淀<过滤<吸附<蒸馏.
4、净水过程中明矾的作用:溶于水产生的胶状物吸附杂质,使杂质沉降。
净水时活性炭的作用:滤去不溶性杂质;吸附一些可溶性杂质;除去臭味
三、硬水和软水
1、硬水:含有较多可溶性钙、镁化合物的水。
软水:不含或含较少可溶性钙、镁化合物的水。软水不一定是纯水,但纯水是软水。
2、鉴别方法:加入肥皂水,若产生大量泡沫的为软水;泡沫较少,甚至有浮渣的为硬水。
3、软化硬水的方法:煮沸或蒸馏。生活中常采用煮沸的方法。
4、硬水的危害:(1)浪费肥皂,洗不净衣服;(2)锅炉用硬水,浪费燃料,甚至引起爆炸。
课题3 水的组成
一、氢气的性质
物理性质:无色、无臭、难溶于水、密度比空气小。
化学性质:可燃性。燃烧方程式:2H2 + O2  2H2O(产生淡蓝色火焰)
2H2O(产生淡蓝色火焰)
注意:混有一定量空气或氧气的氢气遇明火会发生爆炸,因此点燃氢气前一定要验纯。
二、电解水实验
1 现象:正负极都有气体产生,正负极气体体积比为1:2
2 结论:水是氢元素和氧元素组成的。
3 化学反应:2H2O 2H2↑ + O2↑
2H2↑ + O2↑
注意:(1)、电解水实验所用电源为直流电。
(2)、在水中加硫酸钠或氢氧化钠的目的是为了增强导电性。
(3)、H2 和 O2的混合气体称为爆鸣气。爆鸣气是混合物.
三、物质的分类

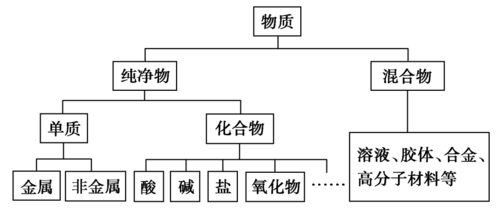
课题4 化学式与化合价
一、化学式
1、化学式的定义:用元素符号和数字的组合表示物质组成的式子。
2、化学式的意义
(1)宏观意义:表示某种物质;表示某种物质的组成。
(2)微观意义:表示1个分子;表示1个分子的构成。
(3)注意:若化学式前面有系数,只表示几个分子。
(4)对比下列符号的意义:
H: ① 氢元素;②1个氢原子。2H:2个氢原子。
H2: ①氢气。②表示氢气由氢元素组成。③1个氢分子。④1个氢分子由2个氢原子构成。
2H2: 表示2个氢分子.
Mg2+:①镁离子;② 1个镁离子带2个单位正电荷;2Mg2+:2个镁离子。
H2O:①表示水; ②表示水由氢元素和氧元素组成;③1个水分子 ;④1个水分子由2个氢原子和1个氧原子构成。
2H2O:表示2个水分子.
二、化合价
1、化合价是元素的化学性质之一。
2、化合价的表示方法:标在元素符号或原子团的正上方。
◆化合价与离子所带电荷的区别与联系。
区别:标的位置不同,正负号与数字的顺序不同。
联系:数值相同,正负号一致。
3、常见元素及原子团的化合价。
一氯钾钠银和氢;二氧钙镁钡和锌;三铝四硅五价磷;
一价氢氧硝酸根;二价碳酸硫酸根; 三价磷酸根;正+1价铵根。
4、化合价规律:
(1)单质中元素化合价为0。
(2)化合物中,正负化合价代数和为0。
(3)原子团中,正负化合价代数和等于原子团化合价。
三、化学式的写法、读法
1、单质写法:除N2、H2、O2、F2、Cl2、Br2、I2外,其余单质直接用元素符号表示。
2、化合物化学式的写法:先排序(正价左,负价右);次注价;后约简;再交叉。
注意:原子团应作为整体,个数超过1时,应用括号。
3 化学式的读法:从后往前读法 “某化某”:不含酸根的化学式。“某酸某”:含酸根的化学式。
四、根据化学式进行的计算。
1、计算组成物质的各元素的原子个数比:等于各元素的脚标比。
注意:(1)元素的顺序按题要求;(2)同一元素多处出现,合并计算。
2、计算物质中各元素的质量比:等于各元素的相对原子质量乘以脚标相比。
注意:CuSO4·5H2O中的 “·”表示相加。
3、计算相对分子质量.等于各元素的相对原子质量乘以脚标相加。
4、计算元素的质量分数:元素的质量分数== Χ 100%
扫描二维码推送至手机访问。
特别声明:
本站属于公益性网站,纯粹个人原因(陪孩子学习便于查询和教授),网站部分内容收集于网络,仅供学生和老师参考、交流使用,请勿用作其他商业收费用途。
如果网站内容能给你带来提升,那便是我经营此网站的初衷。网站相关内容如有问题,请及时提出,我在此谢谢!
本站尊重原创并对原创者的文章表示肯定和感谢,如有侵权请联系删除!针对本站原创内容,本站也欢迎转载,如需转载请注明出处。